TETRALOGIA FALLOTA Tetralogia de Fallot é a cardiopatia congênita cianótica mais comum, bem como uma das primeiras a ter sido corrigida cirurgicalmente.
O diagnóstico de Tetralogia de Fallot pode ser realizado no período pré-natal por ecografia fetal com posterior confirmação com ecocardiografia fetal.
J. M. é o primogênito de pais jovens, casados, classe media, saudáveis e não consanguíneos. A gravidez foi planejada, tendo sido acompanhada pelo PSF. A mãe realizou três ecografias sem alterações. Na ecografia morfológica realizada às 20 semanas e 5 dias de gestação relatou-se uma má visualização dos grandes vasos cardíacos, sem qualquer outra anomalia.
Esse achado justificou a realização de um ecocardiograma fetal às 26 semanas de gestação que relatou: “Comunicação interventricular subaórtica com cavalgamento da aorta sobre o septo interventricular, desproporção entre a artéria pulmonar (2,7 mm) e a artéria aorta (5,2 mm) e válvula pulmonar com fluxo de velocidade elevada (127 cm/seg). Ramos da Artéria Pulmonar confluentes. arco aórtico esquerdo. Boa função biventricular. FCF 130 bpm".
Justifica-se assim a hipótese diagnóstica de Tetralogia de Fallot. O exame complementar foi repetido seis dias depois e confirmou o diagnóstico.
Niels Stenson descreveu o malformação num feto com ectopia cordis (uma malformação congénita rara caracterizada pela localização do coração fora da cavidade torácica do recém-nascido). Na ectopia cordis o coração pode estar localizado na superfície externa anterior (na frente) da cavidade torácica ou deslocado para a cervical ou para o abdómen.
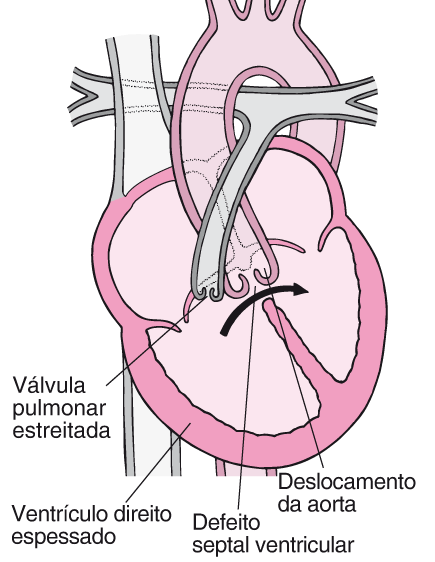
A palavra tetralogia é emprestada, na verdade da literatura, significando geralmente uma historia em 4 (tetra) capitulos, mas o apelido ficou assim mesmo.A tetralogia de Fallot consiste em:
- (1) obstrução na via de saída do ventrículo direito (estenose pulmonar)
- no infundíbulo ventricular direito (área-subpulmonar)
- na valva pulmonar
- atresia pulmonar com CIV forma extrema de tetralogia de Fallot (obstrução completa da via de saída do ventrículo direito)
- (2) comunicação interventricular (CIV)
- (3) dextroposição da aorta cavalgando o septo
- (4) hipertrofia ventricular direita
A etiologia da Tetralogia de Fallot é multifatorial, encontrando-se associada ao:
- consumo materno de ácido retinóico
- diabetes maternos mal controlados
- fenilcetonúria.
Algumas anomalias cromossómicas associam-se também à doença, nomeadamente as trissomias 21 (síndrome de Down), 18 Síndrome de Edwards) e 13 (Síndrome Bartholin-Patau).
Pela possível associação desta cardiopatia a anomalias cromossómicas a mãe do J. M. foi encaminhada para consulta de Genética. No relatório nega-se qualquer deleção ou duplicação patológica num perfil para o sexo masculino. Concluiuse assim que se tratava muito provavelmente de uma cardiopatia isolada não sindromática. Ambos os pais desconhecem a existência de qualquer patologia de carácter heredo-familiar nas suas famílias.
FISIOPATOLOGIA
Quatro alterações anatómicas distintas são presentes na tetralogia Fallot, contudo há de se lembrar, que, na verdade, estas partilham o mesmo defeito embrionário.
A hipertrofia ventricular direita, de fato, é uma resposta secundária ao aumento da pós-carga.
Existem algumas alterações adicionais que surgem com alguma frequência nesta patologia: obstruções ao nível dos ramos da artéria pulmonar, anomalias coronárias, arco aórtico direito e defeitos no septo interventricular adicionais. A valva pulmonar freqüêntemente é bicúspide.
Em caso que os ramos das artérias pulmonares são descontínuos, o fluxo sangüíneo pulmonar pode ser suprido por um canal arterial (ductus arteriosus) patente (PCA) e pelas artérias colaterais aortopulmonares principais que provêm da aorta.
A crista supraventricular é hipertrófica e isso causa estenose infundibular e resulta em uma câmara infundibular de tamanho e contornos variáveis.
O septo aorto-pulmonar tem origem na crista neural, e teria - normalmente - como função separar a artéria aorta das artérias pulmonares. No caso, a porção terminal do septo encontra-se desviada anteriormente e para a direita. Isso impede a fusão adequada do septo interventricular, estreita a saída do ventrículo direito para a artéria pulmonar e alarga a raiz da aorta, com o seu cavalgamento sobre o septo.
A comunicação interventricular geralmente é não-restritiva e é grande. O lugar aonde ela se encontra mais frequentemente é abaixo da valva aórtica. As cúspides aórticas posterior e direita são participantes nesta historia, também. As válvulas mitral e aórtica mantém a continuidade fibrosa normal.
O arco aórtico está do lado direito em 20% dos casos, e a raiz da aorta geralmente é grande e cavalga a CIV em graus variáveis. Quando a aorta acavalga a CIV mais do que 50% e se o músculo estiver separando significativamente a válvula aórtica e o anel mitral (conus subaórtico), esse defeito em geral é classificado como uma forma de ventrículo direito com dupla via de saída (aortica e pulmonar estenotica, sem que isso mude muito a fisiopatologia, que é a mesma da tetralogia de Fallot.
O retorno venoso sistêmico ao átrio direito e ao ventrículo direito é normal.
DISTURBIOS NA HEMODINÂMICA
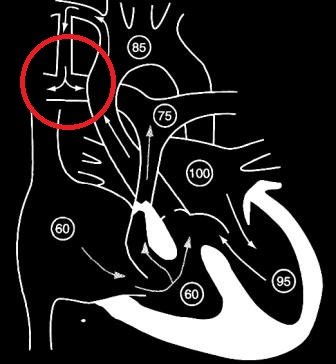
Quando o ventrículo direito se contrai na presença de uma acentuada estenose pulmonar, o sangue passa através da CIV para dentro da aorta, o que resulta em uma dessaturação arterial persistente e cianose.
O fluxo sangüíneo pulmonar, quando gravemente restrito pela obstrução na via de saída do ventrículo direito, pode ser suplementado pela:
- circulação colateral brônquica (ACAPPs)
- por um PCA (no recém-nato)
As pressões sistolica e diastólica de pico em cada ventrículo são semelhantes e se encontram em um nível sistêmico.
Entretanto, a pressão arterial pulmonar é normal ou menor do que o normal.
É fundamental ter em consideração que a apresentação clínica da Tetralogia de Fallot depende do grau de obstrução do trato de saída do ventrículo direito, contribuindo para a considerável variabilidade clínica entre doentes.
A obstrução completa ou quase completa do trato de saída do ventrículo direito resulta numa redução repentina do fluxo pulmonar e em cianose episódica profunda, denominada episódio hipercianóticos, crise de hipóxia ou tet spell.
MANIFESTAÇÃO CLÍNICA
Então, já entendemos que, na verdade, o momento do início dos sintomas e a intensidade da cianose e, depois, o grau de hipertrofia ventricular direita são determinadas pelo grau de obstrução dà via de saída do ventrículo direito.
Se a obstrução for ligeira o fluxo do ventrículo direito irá predominantemente para a artéria pulmonar e apenas uma pequena percentagem passa para a artéria aorta. Os fluxos pulmonar e sistémico serão semelhantes, traduzindo-se em menos episódios cianóticos e clínica menos exuberante.
É descrita, assim, uma forma de tetralogia de Fallot acianótica ou "rósea" que nada mais é que uma obstrução à via de saída do ventrículo direito de leve a moderada (shunt equilibrado está presente através da CIV). Neste tipo de tetralogia Fallot o paciente pode não ser visivelmente cianótico. Nos "hipoxêmicos róseos" a saturação sistêmica pode ser normal
O mais frequente é o aparecimento desta cianose ligeira a moderada no período neonatal, geralmente sem sinais de dificuldade respiratória associados. Esta cianose poderá ser detetada apenas após alguns meses de idade e é mais perceptível nas membranas mucosas dos lábios e da boca e nos leitos ungueais dos dedos das mãos. e dos pés. Porém, na medida que a obstrução aumenta os sintomas (cianose e sopro à auscultação cardíaca) aparecem e prevalecem.
A semiologia classica insistia muito na presença de hipocratismo digital, mas esse é um sinal que hoje aparece menos frequente, por conta da correção cirúrgica que é realizada relativamente cedo.
Em bebês com graus importantes de obstrução do trato de saída do ventrículo direito, a cianose neonatal é notada imediatamente. O fluxo sangüíneo pulmonar pode depender do fluxo através do canal arterial e, pior, se o ductus começar a se fechar nas primeiras horas ou dias de vida, pode ocorrer uma cianose grave e colapso circulatório.
Crianças mais velhas com cianose de longa data que não se submeteram à cirurgia podem ter:
- pele de coloração azul-escura,
- escleróticas cinzentas com vasos sangüíneos ingurgitados
- baqueteamento acentuado dos dedos das mãos e dos pés.
Observa-se, por exemplo, em crianças pequenas com cianose significativa em repouso que estão começando a andar, brincam ativamente por um curto período e então se sentam ou se deitam.
As crianças mais velhas podem ser capazes de caminhar um quarteirão ou pouco mais, antes de parar para descansar.
Caracteristicamente, as crianças assumem uma posição de cócoras para o alívio da dispnéia causada pelo esforço físico; a criança geralmente é capaz de reassumir a atividade física em poucos minutos.
SURGIMENTO DOS EPISODIOS HIPERCIANÓTICOS
Nem todos os doentes apresentam episódios hipercianóticos.
Os episódios hipercianóticos apresentam um quadro clínico distinto:
Estes surgem tipicamente após os dois meses de idade, e o que desencadeia são estados de agitação ou desidratação, podendo ambos exacerbar a obstrução existente.
Um fluxo praticamente inexistente leva a que o sopro presente noutras situações deixe de ser audível. O doente apresenta-se cianótico, polipneico e prostrado.
Surge acidose metabólica que contribui para o aumento da resistência vascular pulmonar, com redução da resistência vascular sistémica.
Há um compromisso do débito cardíaco por isquemia do miocárdio, do qual poderá resultar morte.
O bebê se torna hiperpnéico e inquieto, a cianose aumenta, seguem-se respirações ofegantes e pode ocorrer síncope.
As crises ocorrem com mais freqüência pela manhã, inicialmente, ao acordar ou após episódios de choro vigoroso. O desaparecimento temporário ou uma redução na intensidade do sopro sistólico é habitual, pois o fluxo através da via de saída do ventrículo direito diminui.
As crises podem durar desde poucos minutos até poucas horas, mas raramente o fatais. Depois desses episodios as crianças apresentam fraqueza generalizada e sono.
No paciente moderadamente cianótico em repouso a saturação, em geral, é de 75%-85%.
EPISODIOS HIPERCIANÓTICOs mais graves
Com o tempo e o agravamento, as crises mudam de aspecto. O surgimento de crises graves podem progredir até a perda da consciência e ocasionalmente, convulsões ou hemiparesia. O início geralmente é espontâneo e imprevisível.
As crises estão associadas com a redução do fluxo sangüíneo pulmonar já comprometido, que, quando prolongada, resulta em hipoxia.
Dependendo da freqüência e da gravidade dos ataques hipercianóticos, devem ser instituídos um ou mais desses procedimentos, em seqüência:
- colocação do bebê sobre o abdome (posição de cócoras), com os joelhos encostados ao tórax, enquanto se assegura que a roupa do bebê não faz nenhuma constricção,
- administração de oxigênio (embora o aumento do oxigênio inspirado não reverta a cianose causada pelo shunt intra cardíaco)
- injeção de morfina subcutânea em uma dose que não exceda 0,2 mg/kg.
- Acalmar e segurar o bebê pode abortar a progressão de uma crise em fase inicial
Tentativas prematuras para se obter amostras de sangue podem causar agitação adicional e ser contraproducentes.
Em casos graves (se o surto for extremamente grave e a criança mostrar falta de resposta à terapia em andamento) muito provavelmente o PO2 arterial é menor que 40 mmHg, ou seja, há acidose metabólica com grande perigo. Há necessidade de correção rápida (durante minutos!) com a administração intravenosa de bicarbonato de sódio.
Uma vez que o pH tenha retornado ao normal você já vê recuperação da "crise" que, em geral, é rápida. Além disto, precisa fazer medidas repetidas do pH sangüíneo, pois pode ocorrer uma rápida recorrência da acidose.
Uma alternativa corjaosa e temerária em caso que você não encaminhou já o bebê para UTI é administrar drogas intravenosas cuja finalidade, na verdade é aumentar a resistência vascular sistemica, melhorar o efluxo do ventrículo direito e diminuir o shunt direito-esquerdo
O bloqueio beta-adrenérgico pela administração intravenosa de propranolol (0,1 mg/kg dado lentamente, até um máximo de 0,2 mg/kg) também é útil.
Em caso de tetralogia de Fallot grave não-tratada em particular quando a saturação de oxigênio é cronicamente menor do que 70% o crescimento e o desenvolvimento podem ser retardados, inclusive a puberdade (também pode ser retardada em pacientes que não se submetem à cirurgia).
Devido a uma hipertrofia ventricular direita o hemitórax anterior esquerdo pode se deformar, sendo mais convexo para anterior.
O pulso geralmente é normal, assim como a pressão venosa e a arterial. Como o fluxo no defeito interventricular é geralmente não turbulento, este não origina sopros audíveis.
Na ausculta sempre ouvimos um sopro sistólico mais intenso na borda estemal esquerda, com timbre alto e rude. Ele é causado pela turbulência através da via de saída do ventrículo direito.
A evolução desse sopro pode parecer paradoxal - ele tende a se tornar mais alto, mais longo e mais rude conforme a gravidade da estenose pulmonar aumenta de leve a moderada, mas quando há, de repente, obstrução grave com hipoxia ele pode se tornar menos evidente.
DIAGNÓSTICO
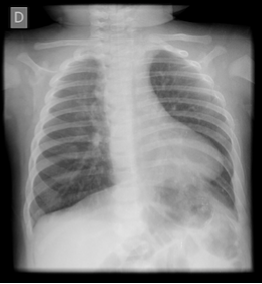
Após a suspeita clínica de Tetralogia de Fallot recomenda-se a realização de eletrocardiograma e radiografia torácica.
O primeiro exame complementar deve revelar um desvio do eixo para a direita e uma proeminente hipertrofia ventricular direita, com ondas R amplas nas derivações precordiais direitas e ondas S amplas nas derivações precordiais esquerdas.
O Rx pode mostrar o aspecto de "coeur en sabot", uma expressão já classica que compara silhueta cardíaca à de uma botina ou um tamanco. O ventrículo direito hipertrofiado causa uma sombra apical arredondada com a ponta levantada para cima, de modo que ela está situada mais alta do que o normal acima do diafragma.
Ao 36º dia de vida após consulta de Neonatologia o J. M. foi referenciado ao Serviço de Urgências Pediátrico por dificuldade respiratória e má progressão ponderal - aumentou apenas 170g em cerca de um mês.
Na admissão apresentava-se com um peso de 2610g, apirético, FC 170 bpm, FR 35 cpm, SpO2 100% ar ambiente, estridor intermitente e tiragem intercostal. Com parâmetros de infeção negativos.Na admissão em internamento realizou-se ecocardiograma que relatou uma Tetralogia de Fallot com boa anatomia, sem necessidade de intervenção naquele momento. Pela existência de arco aórtico direito foi sugerida a exclusão de anel vascular associado, que justificaria a clínica de obstrução alta. Neste contexto foi internado na Unidade de Pneumologia Pediátrica para esclarecimento do quadro e monitorização cardiopulmonar.
Durante o internamento foram realizados exames complementares para investigação diagnóstica. Destaca-se a Angio TAC, que relata a presença de arco aórtico direito de tipo I, redução difusa do calibre do tronco da artéria pulmonar, com permeabilidade pulmonar mantida e defeito do septo interventricular adjacente à emergência da aorta. Não se observaram anéis vasculares nem sinais de significativa compressão extrínseca. Destaca-se também a broncofibroscopia, que diagnosticou uma laringomalácia T1 e T4, com compressão extrínseca da traqueia (pelo arco direito).
Apesar de ser uma das cardiopatias congénitas mais frequentes, a Tetralogia de Fallot apresenta uma das menores taxas de diagnóstico pré-natal.
A ecocardiografia, seja ela durante a vida fetal ou depois do nascimento é considerada o instrumento essencial para o diagnóstico.
Na verdade, a ecocardiografia fetal detalha todas as patologias cardiovasculares no feto. Esta deve ser realizada entre as 18 e as 22 semanas a qualquer grávida com um risco aumentado de cardiopatia congénita.
A ecocardiografia bidimensional depois do nascimento estabelece o diagnóstico e fornece informações sobre a anatomia que define a lesão. Assim, vamos poder avaliar:
- a extensão do acavalgamento da aorta sobre o septo
- a localização e o grau de obstrução da via de saída do ventrículo direito
- o tamanho das artérias-ramos das artérias pulmonares
- o tamanho do arco aóriico
- a existência dum PCA (poderia suprir uma porção do fluxo sangüíneo pulmonar)
O ecocardiograma pode dispensar a necessidade de um cateterismo.
Porém, quando o cateterismo se faz necessário, ele vai demonstrar:
- pressão sistolica no ventrículo direito igual à pressão sistêmica
- pressão arterial pulmonar geralmente é menor do que o normal
- pressão na artéria pulmonar acentuadamente diminuída
A ventrículografia direita seletiva demonstra melhor a anatomia da tetralogia de Fallot.
A arteriografia também pode definir varios trajetos das arterias coronarias.
PROGNOSTICO E COMPLICAÇÕES
Aos 6 meses e 19 dias de vida foi internado para tratamento cirúrgico eletivo. Foi submetido a encerramento da Comunicação Interventricular com patch de Dacron, recessão de bandas do ventrículo direito e alargamento do anel valvular com patch transvalvular. Adicionalmente foi efetuada secção de ligamento arterial e pexia de tronco braquicefálico esquerdo para libertação do anel vascular. A cirurgia decorreu com tentativa de valvuloplastia direta da válvula pulmonar que foi ineficaz, tendo-se avançado para cirurgia convencional de alargamento da câmara de saída.
Complicações graves se constituem em risco para os pacientes com tetralogia de Fallot, em caso que a correção não estará feita.
A maioria das crianças que realiza reparação completa da Tetralogia de Fallot tem um pós-operatório curto, tendo alta cerca de uma semana após a cirurgia.
TROMBOSE CEREBRAL
Uma complicação temida mais freqüentemente em pacientes com menos de dois anos - tromboses cerebrais nas veias cerebrais ou nos seios durais - é uma eventualidade lastimavel em caso da presença de extrema policitemia e desidratação.
Na verdade, esses pacientes podem ter anemia por deficiência de ferro. Os níveis de hemoglobina e de hematócrito muitas vezes são dentro da variação normal.
A terapia nos pacientes extremamente policitêmicos consiste em:
- hidratação adequada
- medidas de suporte
- sangria
- reposição volumétrica com plasma fresco congelado
A heparina tem pouco valor, e é contra-indicada em pacientes com infarto cerebral hemorrágico. A fisioterapia deve ser instituída o mais rápido possível.
ABSCESSO CEREBRAL
São menos comuns (extremamente raros quando a maioria dos pacientes realiza as correções bem cedo, na infância).
Diferente do caso das tromboses, os pacientes com abscessos cerebrais geralmente têm mais de dois anos.
Como inicía?
FORMA LENTA: O início da doença freqüentemente é insidioso e consiste em febre baixa ou alterações graduais no comportamento, ou em ambos.
FORMA RÁPIDA: Alguns pacientes têm um início agudo dos sintomas, que podem se desenvolver após história recente de cefaléia, náusea e vômitos. As convulsões podem ocorrer; sinais neurológicos localizados dependem da localização e do tamanho do abscesso e da presença de uma pressão intracraniana aumentada.
A TC ou a IRM confirma o diagnóstico. A terapia antibiótica pode ajudar a manter a infecção localizada, mas a drenagem cirúrgica do abscesso geralmente é necessária.
ENDOCARDITE BACTERIANA
A endocardite é um verdadeiro problema, primeiro, porque complica os shunts paliativos, qualquer estenose pulmonar residual ou CIV. Tem predileta para infundíbulo do ventrículo direito, valva pulmonar, aórtica ou, raramente, tricúspide.
A profilaxia antibiótica é essencial antes e após os procedimentos dentários e certos procedimentos cirúrgicos associados a uma elevada incidência de bacteremia.
A insuficiência cardíaca não é uma característica comum em pacientes com tetralogia de Fallot. Ela pode ocorrer em um bebê pequeno com tetralogia de Fallot "rósea" ou acianótica. Conforme o grau de obstrução pulmonar piora com a idade, o paciente experimenta cianose, freqüentemente por volta de 6-12 meses de idade. Nesse período, esses pacientes se encontram sob maior risco de crises de hipoxemia.
O pós-operatório imediato foi complicado por quadro de insuficiência cardíaca de baixo débito sistémico, com impacto multiorgânico, tendo desenvolvido insuficiência renal, hepática e respiratória, derrames com necessidade de tratamento médico e paracenteses. Em D8 do pós-operatório realizou-se cateterismo diagnóstico que demonstrou Comunicação Interventricular residual grande com indicação cirúrgica e obstáculo residual moderado.
Após encerramento da CIV residual verificou-se evolução favorável, recuperando lentamente da disfunção multiorgânica. À data de alta não apresentava sintomas cardiovasculares, encontrando-se sem sinais e insuficiência cardíaca. Teve alta com terapêutica farmacológica de furosemida e espironolactona. As avaliações ecocardiográficas foram compatíveis com um bom resultado cirúrgico
ANOMALIAS ASSOCIADAS
- PCA
- defeitos no septo atrial
- arco aórtico à direita, e outras anomalias das artérias pulmonares e do arco aórtico
- persistência de uma veia cava superior esquerda drenando para o seio coronário
- múltiplas CIVs
- defeito septal atrioventricular, freqüentemente associado à síndrome de Down
- ausência congênita da valva pulmonar
- ausência de um dos ramos da artéria pulmonar
- complexo CATCH22
Como uma das malformações conotruncais, a tetralogia de Fallot pode estar associada ao espectro de lesões conhecidas como CATCH 22 (defeitos cardíacos, fácies anormal, hipoplasia timica, fenda palatina (deft), hipocalcemia). A CATCH 22 inclui pacientes com características clínicas da síndrome de DiGeorge (hipocalcemia, hipoplasia tímica, discretas anomalias faciais) ou da síndrome velocardiofacial de Shprintzen (fácies anormal, fenda palatina). A análise citogenética utilizando a hibridização fluorescente in situ demonstra deleções de um segmento do cromossomo 22q11 conhecido como a região crítica de DiGeorge.
A presença de microdeleções 22q11 é sugestiva de alguns síndromes, sendo o Síndrome de DiGeorge o mais grave – caracteriza-se por anomalia palatina, fácies dismórfica, défice cognitivo, imunodeficiência e/ou hipocalcémia.
O Síndrome de Shprintzen (velocardiofacial) é uma microdeleção 22q11 menos severa, não incluindo a imunodeficiência e hipocalcémia da patologia anterior.
TRATAMENTO
O tratamento da tetralogia de Fallot depende da gravidade da obstrução do trato de saída do ventrículo direito.
Cerca de metade das crianças com Tetralogia de Fallot tem risco de morrer no primeiro ano de vida se a cirurgia corretiva não é feita.
Uma pessoa com tetralogia Fallot raramente ultrapassa 30 anos de idade se o defeito não for solucionado.
Se não for corrigida cirurgicamente, a Tetralogia de Fallot é potencialmente fatal, com probabilidades de sobrevivências a um, três e dez anos de 66%, 49% e 24%, respetivamente.
Existem descrições de casos isolados de sobrevivência até às oitavas e nonas décadas de vida sem cirurgia.
A correção cirúrgica tem como objetivos:
- o encerramento da comunicação interventricular,
- a preservação da forma e função do ventrículo direito
- trato de saída associado a uma válvula pulmonar intacta (o mais dificil de se conseguir)
Antes, a tecnica utilizada era com accesso pela ventriculotomia direita (cicatrização e disfunção complicadas), porém, nas últimas décadas a abordagem transauricular-transpulmonar conquistou cada vez mais espaço.
CASOS GRAVES
Os bebês com tetralogia grave precisam de tratamento médico e intervenção cirúrgica no período neonatal.
O bebê deve ser transportado para um centro médico adequadamente equipado para avaliar e tratar os neonatos com doença cardíaca congênita sob as melhores condições.
Manter a oxigenação e uma temperatura corporal normal são requerimentos óbvios, porque:
- Uma hipoxia prolongada e grave pode levar a choque, insuficiência respiratória e acidose intratável, mesmo quando estejam presentes lesões passíveis de cirurgia.
- O frio aumenta o consumo de oxigênio, o que coloca um estresse adicional sobre um bebê cianótico, cuja liberação de oxigênio já é limitada.
Os bebês com sintomas e cianose grave no primeiro mês de vida apresentam uma acentuada obstrução na via de saída ventricular direita ou atresia pulmonar. Estão disponíveis duas opções nesses bebês:
- A primeira é um shunt paliativo sistêmico - artéria pulmonar, realizado para aumentar o fluxo sangüíneo da artéria pulmonar. O argumento a favor dessa cirurgia, antigamente a única opção para estes pacientes, é diminuir o grau de hipoxia e melhorar o crescimento linear, assim como aumentar o crescimento dos ramos das artérias pulmonares.
- A segunda opção é a cirurgia corretiva com o coração aberto realizada no início da infância, e mesmo no período neonatal em bebês criticamente enfermos (obteve uma aceitação mais ampla)
A terapia tem como objetivo fornecer um aumento imediato do fluxo sangüíneo pulmonar para prevenir as seqüelas da hipoxia severa.
Os níveis de glicose sangüínea devem ser monitorizados, pois é mais provável a ocorrência de hipoglicemia em bebês com doença cardíaca congênita.
Os bebês com obstrução acentuada da via de saída do ventrículo direito podem deteriorar rapidamente, pois conforme o canal arterial (ductus arteriosus) começa a se fechar, o fluxo sangüíneo pulmonar é ainda mais comprometido.
Fica, então, necessária, a administrtração intravenosa - assim que se suspeitar de uma doença cardíaca congênita! - de prostaglandina E2 (0,05-0,20 mcg/kg/min) para garantir o fluxo sangüíneo pulmonar adequado até que possa ser realizada a cirurgia cardíaca - por isso, a infusão deverá ser continuada durante todo o período pré-operatório e durante o cateterismo cardíaco. A prostaglandina é:
- relaxante potente e específico do músculo liso ductal
- vasodilatador do canal arterial
Pós-operatoriamente, a infusão pode ser continuada brevemente, como um vasodilatador pulmonar, para aumentar o fluxo através de um shunt paliativo ou através de uma valvulotomia cirúrgica.
Quando um bebê apresenta sintomas e cianose grave no primeiro mês de vida, você como profissional precisa pensar que há uma acentuada obstrução na via de saída ventricular direita. Ou, talvez, até uma atresia pulmonar.
Ou seja, a pressão ventricular direita é muito alta, entretanto, como há CIV, o sangue tem só a opção dessa comunicação. Ela descarrega o VD de tarefa hemodinâmica, entretanto, mistura muito o sangue oxigenado com aquele venoso e daí a cianose que você vai ver.
A lógica que segue - o tratamento teria duas opções: ou você alarga o orificio da arteria pulmonar (mas isso seria dificil e não resolveria a questão do shunt - a CIV ainda está lá), ou você CRIA outro shunt que seria mais "saudável" que o desvio pela CIV.
A PRIMEIRA OPÇÃO: O SHUNT PALIATIVOIsso é o shunt paliativo sistêmico-artéria pulmonar, realizado para aumentar o fluxo sangüíneo da artéria pulmonar. A primeira dentre as duas opções cirurgicas.
Antes da epoca moderna essa cirurgia era a única opção para estes pacientes.
A literatura afirma que os beneficios dessa cirurgia constariam em:
- diminuir o grau de hipoxia
- melhorar o crescimento linear
- aumentar o crescimento dos ramos das artérias pulmonares
CIRURGIA COM CORAÇÃO ABERTOBem, em princípio, essa é a opção para os casos que poderiam esperar, realizada no início da infância. Mas não é impossível realizar ela já mesmo no período neonatal em bebes criticamente enfermos.
Parece que obteve uma aceitação mais ampla e os excelentes resultados a curto e médio prazos são incentivadores.
As vantagens da cirurgia corretiva no início da infância versus um shunt paliativo e correção mais tardiamente na infância ainda estão sendo debatidas.
CASOS MODERADOS E LEVES
Esses casos são, na maioria estáveis e aguardando intervenção cirúrgica porém precisam de uma cuidadosa observação. Em bebês com cianose menos intensa, que podem ser mantidos com bom crescimento e ausência de crises de hipoxemia, a correção primária é realizada eletivamente entre os quatro e 12 meses de idade.
Assim como foi remarcado um pouco acima, é necessário evitar uma das mais perigosas situações - a desidratação. A prevenção ou o tratamento imediato da desidratação é importante para evitar hemoconcentração e possíveis episódios trombóticos.
Crises de hipoxemia podem aparecer, especialmente se tiver uma deficiência relativa de ferro - a terapia com o ferro pode diminuir sua freqüência e também melhorar a tolerância ao exercício e o bem-estar em geral.
O propranolol oral (0,5-1,0 mg/kg a cada seis horas) pode diminuir a freqüência e a severidade das crises hipercianóticas.
Em bebês com cianose menos intensa, que podem ser mantidos com bom crescimento e ausência de crises de hipoxemia, a correção primária é realizada eletivamente entre os quatro e 12 meses de idade.
PROCEDIMENTOS
O SHUNT BLALOCK-TAUSSIG
Na verdade, é um conduto de Gore-Tex anastomosado lado a lado da artéria subclávia para o ramo homolateral da artéria pulmonar, ou como variante chamada shunt central, da aorta ascendente para o tronco da artéria pulmonar
Pode ser realizada com sucesso no período neonatal com shunts de 3-4 mm de diâmetro, e também foi executada com sucesso em bebes prematuros*.
Complicações:
- quilotórax - necessita de toracocenteses repetidas e, ocasionalmente, reoperação para a ligadura do dueto torácico
- paralisia diafragmática - pode resultar em evolução pós-operatória mais difícil. Suporte ventilatório prolongado e fisioterapia vigorosa podem ser necessários, mas a função diafragmática geralmente retorna em 1-2 meses;
- a síndrome de Horner geralmente é temporária e não precisa de tratamento.
O curso pós-operatório dos pacientes com um procedimento de shunt bem-sucedido é relativamente sem eventos. As complicações pós-operatórias podem ocorrer após uma toracotomia lateral.
RESULTADOS
Após um procedimento de shunt bem-sucedido, a cianose diminui.
Porém, conforme a criança cresce, mais fluxo sangüíneo pulmonar é necessário, e o shunt eventualmente se toma inadequado.
Ás vezes se desenvolve uma cianose progressivamente mais intensa.
Neste caso:
- se a anatomia for favorável deve ser realizada uma cirurgia corretiva
- se houver ramos hipoplásicos nas artérias pulmonares ou se o primeiro shunt durar apenas um breve período em um bebê pequeno, uma segunda anastomose aortopulmonar pode ser necessária no lado oposto
- vários grupos relataram paliação bem-sucedida da tetralogia de Fallot em bebês pela valvoplastia pulmonar com balão
CIRURGIA CORRETIVA COM CORAÇÃO ABERTO
O risco cirúrgico da correção total é menor que 5%. A técnica inclui:
- qualquer shunt sistêmico-pulmonar previamente estabelecido precisa ser obliterado antes da correção completa
- remoção dos feixes musculares obstrutivos (alívio da obstrução)
- fechamento com patch da CIV (parar a mistura do sangue)
- valvotomia se a válvula pulmonar for estenótica
- patch transanular através do anel valvar pulmonar (anel da valva pulmonar pequeno)
Uma ventriculotomia direita era a abordagem-padrão; no entanto, uma abordagem transatrial-transpulmonar pode ser usada para reduzir os riscos a longo prazo de uma ventriculotomia.
Após uma correção total bem-sucedida, os pacientes geralmente são assintomáticos e capazes de viver suas vidas sem restrições.
Os problemas pós-operatórios imediatos incluem:
- sangramento aumentado
- insuficiência ventricular direita,
- bloqueio atrioventricular transitório,
- CIV residual com shunt esquerdo-direito,
- infarto do miocárdio pela interrupção de uma artéria coronária aberrante
- aumento desproporcional na pressão atrial esquerda devido às colaterais brônquicas residuais
- insuficiência valvar pulmonar isolada, induzida cirurgicamente - geralmente bem tolerada
- insuficiência cardíaca pós-operatória - agente inotrópico positivo, como a digoxina. O
Os distúrbios de condução podem ocorrer após a cirurgia. O nó atrioventricular e o feixe de His e as suas divisões estão muito próximos à CIV e podem ser lesados durante a cirurgia.
- bloqueio atrioventricular permanente - colocação de um marcapasso definitivo
- bloqueio atrioventricular transitório no período pós-operatório imediato
- bloqueio do ramo direito - bastante comum no eletrocardiograma pós-operatório
Numerosas crianças têm extra-sístoles ventriculares após a correção da tetralogia de Fallot.
ACOMPANHAMENTO PÓS-OPERATÓRIO:
- Estudos de monitorização eletrocardiográfica de 24 horas (Holter) devem ser realizados para assegurar que episódios curtos e ocultos de taquicardia ventricular não estejam ocorrendo.
- Estudos com teste ergométrico podem ser úteis na provocação das arritmias cardíacas que não sejam aparentes em repouso.
- Na presença de arritmias ventriculares complexas ou anormalidades hemodinâmicas residuais graves, justifica-se a terapia antiarrítmica profilática.
- Nova cirurgia é indicada se estiver presente uma obstrução significativa na via de saída do ventrículo direito ou uma insuficiência pulmonar severa.
MISODOR, 26 DE JANEIRO DE 2019
BIBLIOGRAFIA:
- Clínica Universitária de Pediatria Clique aqui para identificar a Unidade Orgânica Tetralogia de Fallot – Um Desafio Multidisciplinar Mariana Carregueiro Barreira TRABALHO FINAL MESTRADO INTEGRADO EM MEDICINA, disponivel no endereço eletronico http://repositorio.ul.pt/bitstream/10451/32306/1/MarianaCBarreira.pdf, accessado dia 12 de janeiro de 2018.
- Nelson Tratado de Pediatria Por Robert Kliegman, Bonita M.D. Stanton, Joseph St. Geme, Nina F Schor VOL II
- Apitz C, Webb GD, Redington AN. Tetralogy of Fallot. Lancet. 2009;374(9699):1462-1471. doi:10.1016/S0140-6736(09)60657-7.
- Fernando MORAES NETO, Cláudio A. GOMES, Cleusa LAPA, Sheila HAZIN, Euclides TENÓRIO, Sandra MATTOS, Carlos R. MORAES - Tratamento cirúrgico da tetralogia de Fallot no primeiro ano de vida
- Sonia F. Mesquita, Raquel Snitcowsky (in memoriam), Antonio Augusto Lopes Estrutura e Função Ventricular Direita como Possíveis Determinantes do Resultado Cirúrgico após Trinta Anos de Correção da Tetralogia de Fallot
Todos os direitos reservados. 2026.
A VITÓRIA É SOMENTE SUA! O CAMINHO É NOSSO!
O site misodor.com.br está online desde 04 de novembro de 2008
O nome, o logo e o site MISODOR são propriedade declarada do webmaster
Qualquer conteudo deste site pode ser integralmente ou parcialmente reproduzido, com a condição da menção da fonte.